Données expérimentales et équations du viriel
Détermination expérimentale des coefficients du viriel
La forme de l'équation du viriel (l'expansion en densité) :
En définissant le facteur de compressibilité Z,
On détermine aisément :
Remarque : Quelques remarques
Ces expressions pour les coefficients du viriel nécessitent des données très précises à très basse densité (phase gaz).
En pratique, le second coefficient B est connu avec précision. C est connu avec moins de précision., D encore moins, etc.
Comparaison avec l'expérience des expansions de la pression en série de la densité (équation du viriel) tronquée à plusieurs ordres
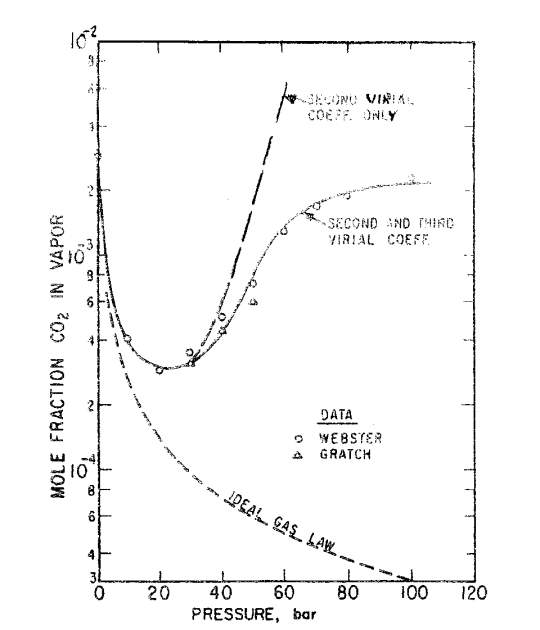
La figure ci-dessous compare l'effet de la troncature à l'ordre 1 (équation des gaz parfait ; B = C = D = ... = 0) à l'ordre 2 (C = D = ... = 0) et à l'ordre 3 (D = ... = 0).
Les coefficients sont calculés à l'aide du potentiel de Kihara (un potentiel de Lennard-Jones où les molécules sont considérées comme des sphères de rayon non nul et qui prédit mieux les coefficients du viriel que celui de Lennard Jones).
Il est préférable de ne pas tronquer : l'équation du gaz parfait (tronquée à l'ordre 1) ne prédit pas le minimum de solubilité avec la pression. La troncature au troisième ordre améliore très significativement celle au deuxième ordre pour les hautes pressions.
Ordre de grandeur
Le tableau ci-dessous décrit l'ordre de grandeur de la correction apportée par chaque coefficient pour le facteur de compressibilité de l'argon à 25°C :
pression P (atm) | facteur de compressibilité Z |
1 | 1 - 0,00064 + 0,00000 +.... (+0,00000) |
10 | 1 - 0,00648 + 0,00020 +.... (-0,00007) |
100 | 1 - 0,06754 + 0,02127 +.... (-0,00036) |
1000 | 1 - 0,38404 + 0,68788 +.... (+0,32272) |
à 10 atm, la correction apportée par le troisième coefficient C (0,00020) est encore marginale et la correction de B reste faible.
A 100 atm, les corrections de B et C sont significatives, mais suffisent.
à 1000 atm, non seulement les corrections de B et C sont très importantes mais elle sont insuffisantes car le reste à corriger est du même ordre de grandeur (+0,32272).
Comparaison avec l'expérience des expansions de la pression en série de la densité (équation du viriel) et en série de la pression
La figure ci-dessous présente le facteur de compressibilité de l'argon à -70°C et la troncature des deux séries à l'ordre 3 (D = 0 ou D' = 0) :
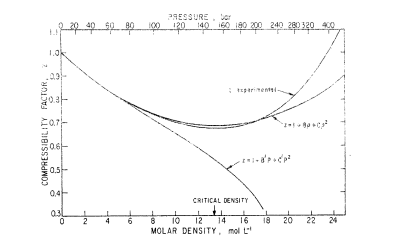
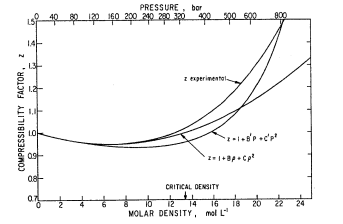
On note l'avantage certain de l'équation du viriel (la série en densité) par rapport à la série en pression, même si à haute température (25°C), la série en pression est plus en accord avec les mesures expérimentales.
Domaine de validité
Pourvu que l'on dispose des valeurs de coefficients, l'équation du viriel est généralement valide :
en dessous de la température critique, l'accord est bon jusqu'à la pression de vapeur saturante, mais mauvais pour le volume molaire liquide.
au dessus de la température critique, l'équation est valide jusqu'à la densité molaire critique, mais nécessite au moins 4 ou 5 coefficients dans ce cas.
Les cas évidents de non validité de l'équation du viriel sont :
le système ne peut plus être décrit comme des molécules individuelles : ex. association en phase vapeur de l'acide acétique ;
les interactions sont décrites par des potentiels ayant une portée plus longue que 1/r3 : ex. interactions entre ions de type coulombiennes en 1/r.