Présentation du modèle
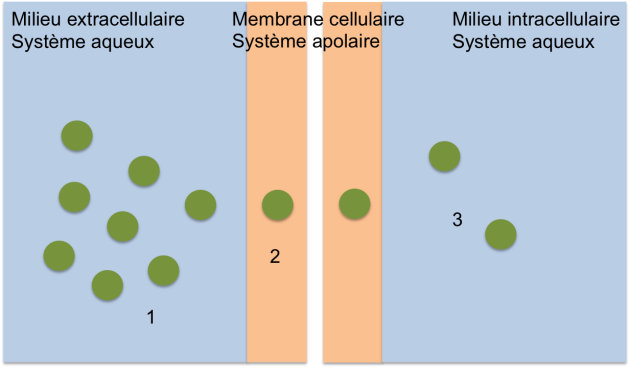
La diffusion passive est un mécanisme de passage membranaire très important et très fréquent. Le modèle repose sur les propriétés physico-chimiques à la fois du xénobiotique et des milieux dans lesquels se trouve le xénobiotique. En effet, les milieux extra-cellulaire et intracellulaire sont aqueux, alors que la membrane cellulaire est constituée d'une bicouche lipidique. Le xénobiotique doit donc avoir de l'affinité à la fois pour le système aqueux et pour les lipides de la membrane cellulaire.
Il est possible de diviser ce modèle en plusieurs étapes :
1 : le xénobiotique libre, solubilisé dans le système aqueux se trouve d'un côté de la membrane.
2 : le xénobiotique passe du système aqueux au système lipidique de la membrane cellulaire. Il reste libre et solubilisé dans la bicouche lipidique.
3 : le xénobiotique passe du système lipidique de la membrane au système aqueux de l'autre côté de la membrane cellulaire.
On observe, à chaque fois, un changement de phase. La solubilité du xénobiotique dans les systèmes aqueux et lipidique est fondamentale. Par conséquent, il est important de connaître les mécanismes moléculaires expliquant la solubilisation d'un composé pour pouvoir déterminer, en fonction de sa structure, sa solubilité dans un système aqueux (hydrosolubilité) et sa solubilité dans un système lipidique (liposolubilité).
L'hydrosolubilité et la liposolubilité ne sont pas des propriétés opposées. Il existe des substances à la fois hydrosolubles et liposolubles, comme par exemple l'éthanol qui est généralement présenté dans une solution aqueuse et qui peut, après absorption par l'organisme, se retrouver dans les membranes des neurones et provoquer des troubles du comportement. Il existe également des substances hydrosolubles mais pas liposolubles ou inversement liposolubles mais non hydrosolubles. Enfin, il existe des substances qui ne sont ni hydrosolubles, ni liposolubles et qui servent par exemple à fabriquer des contenants pour l'eau ou l'huile.
Rappel : solubilité d'une substance
Un composé est soluble dans un solvant s'il a de l'affinité pour ce solvant, c'est à dire s'il peut établir des liaisons non covalentes avec le solvant. Il existe plusieurs catégories de liaisons non covalentes qui dépendent de la polarité des liaisons covalentes des molécules impliquées.
On définit classiquement trois types de liaisons non covalentes :
les interactions ioniques,
les liaisons hydrogènes
les liaisons de Van Der Waals.
La substance solubilisée est appelée soluté et le résultat de la solubilisation d'un soluté dans un solvant est une solution. Plus le soluté peut établir des interactions non covalentes avec le solvant, plus il est soluble dans ce solvant.
les interactions ioniques
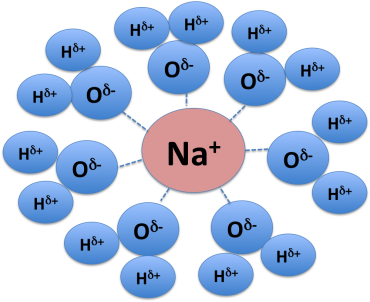
Elles s'établissent entre deux ions de charges opposées, mais elles peuvent également s'établir entre un ion et un grand nombre d'atomes d'eau, molécule fortement polarisée. Par exemple, un ion sodique, Na+ établit des interactions ioniques avec "n" molécules d'eau. Les interactions ioniques peuvent être très fortes : l'énergie mise en jeu varie de quelque dizaines de kJ/mol à plusieurs centaines de kJ/mol.
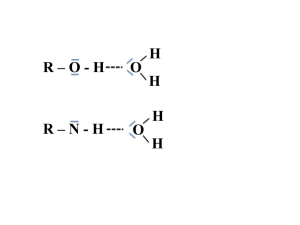
les liaisons hydrogènes
Elles s'établissent entre un atome d'hydrogène lié à un atome très électronégatif d'une molécule et un doublet non liant d'un atome électronégatif, le plus souvent les atomes O et N, d'un autre groupement moléculaire.
les interactions de Van Der Waals
Elles font intervenir trois phénomènes intermoléculaires : des interactions de type dipôle permanent - dipôle permanent, des interactions de type dipôle permanent dipôle induit et des interactions de type dipôle induit dipôle instantanée.
Classiquement, les interactions de type Van Der Waals s'établissent entre des molécules présentant des liaisons covalentes de type - CH2-CH2- (par exemple entre des alcanes). Ces interactions sont très faibles, de l'ordre du kJ/mol, mais plus la molécule est importante, plus le nombre d'interactions de type Van Der Waals qu'elle pourra faire sera grand.
Les lipides des membranes cellulaires réalisent essentiellement ce type d'interaction.
Les ions de petite taille ne peuvent pas établir ces interactions. Un ion n'a aucune affinité pour les lipides, il n'est pas liposoluble. Par conséquent, une molécule ionisée ne pourra pas traverser par diffusion passive une membrane cellulaire.
Fondamental :
Dans un système aqueux, les interactions ioniques et hydrogènes sont importantes, alors que dans un système apolaire (ex : les membranes cellulaires), les interactions de Van Der Waals deviennent importantes.
Modélisation de la diffusion passive : la loi de Fick
La vitesse de diffusion est modélisée par la loi de Fick :
S : surface de la membrane
Ce : concentration extra-cellulaire
Ci : concentration intracellulaire
K = coefficient de la perméabilité de la membrane
Ce coefficient dépend de plusieurs paramètres :
le coefficient de diffusion (Kdiff)
le coefficient de partition eau / octanol (Kow)
Kow est un coefficient très important. Il est déterminé en faisant le rapport de la concentration maximale d'un composé solubilisé dans l'eau sur la concentration maximale du même composé solubilisé dans un solvant apolaire. Le solvant apolaire de référence est l'octanol qui est censé être représentatif des lipides de la bicouche lipidique. Il donne une indication sur la solubilité du composé. Plus il est important, plus le composé à de l'affinité pour les systèmes apolaires. Mais il est important de retenir qu'il correspond à un rapport. Pour bien apprécier ce paramètre, il est important de connaître en plus au moins une des deux solubilités.
l'épaisseur de la membrane (d)
Les conséquences pratiques de la loi de Fick
La possibilité et l'importance d'une diffusion passive dépend de certaines caractéristiques provenant du xénobiotique et de la membrane impliquée.
Caractéristiques dépendant du xénobiotique :
solubilité dans l'eau et dans les lipides
Comme cela a été dit plus haut, le xénobiotique doit être à la fois soluble dans l'eau et dans les lipides pour pouvoir diffuser au travers d'une membrane cellulaire.
poids moléculaire
Le xénobiotique ne doit pas présenter un poids moléculaire trop grand. A partir d'un poids moléculaire supérieur à 500, l'efficacité de la diffusion passive diminue.
gradient de concentration
La diffusion passive ne consomme pas d'énergie. C'est la différence de concentrations de part et d'autre de la membrane qui permet le phénomène. Si les concentrations sont identiques des deux côtés de la membrane, la diffusion passive s'arrête.
Caractéristiques dépendant de la membrane :
superficie de la surface membranaire
La superficie de la membrane influence l'efficacité de la diffusion passive. Plus la superficie est élevée, plus la vitesse de diffusion passive sera grande.
temps de présence
Plus le xénobiotique reste présent au niveau de cette membrane, plus l'efficacité de la diffusion passive sera grande.
Par contre la diffusion passive n'est pas un phénomène spécifique : il n'y a pas reconnaissance entre le xénobiotique et la membrane. Elle ne peut pas être saturée. Enfin, elle ne fait pas appel à un apport d'énergie.
Un cas particulier : le piégeage ionique
Le piégeage ionique est la conséquence de l'absence de solubilité d'une forme ionisée à l'intérieur des membranes cellulaires. Le piégeage ionique peut s'observer avec des acides faibles ou des bases faibles, c'est à dire des molécules qui, en fonction du pH, sont soit majoritairement ionisées, soit majoritairement non ionisées. Il s'observe donc quand le pH varie de part et d'autre d'une membrane cellulaire.
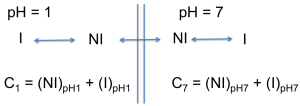
On considère un acide faible (AH), acide carboxylique dont le pKa = 3. Il est en équilibre avec sa base conjuguée (A-). On considère deux systèmes aqueux de pH différents séparés par une membrane cellulaire. Le pH d'un système est égal à 1, le pH de l'autre système est de 7. La concentration totale correspond à la somme de la concentration de la forme non ionisée (notée ici NI) et la concentration de la forme ionisée (notée I).
La formule de Handerson-Hasselbach exprime le pH en fonction du pKa et des concentrations de la base et de l'acide.
Grâce à cette équation, il est possible d'exprimer la concentration de la forme ionisée en fonction de la concentration de la forme non ionisée, du pH et du pKa.
soit :
La concentration totale du xénobiotique est égale à la somme des concentrations de la forme ionisée et de la forme non ionisée.
Il est possible d'exprimer cette concentration totale en fonction de la concentration de la forme non ionisée.
On fait alors le rapport des concentrations totales :
Si on se place à l'équilibre, la concentration de la forme non ionisée dans le système à pH = 1 est identique à la concentration de la forme non ionisée dans le système à pH = 7 (rappel : seule la forme non ionisée peut franchir la membrane cellulaire).
Quand le système atteint l'équilibre (c'est à dire que les concentrations de la forme non ionisée sont identiques des deux côtés de la membrane), ont obtient que la concentration totale du xénobiotique dans le système à pH 7 est environ 10 000 fois plus importante par rapport à la concentration totale dans le système à pH 1.
Ce phénomène s'explique par le déplacement de l'équilibre acido-basique en faveur de la base conjuguée (c'est à dire de la forme ionisée dans notre exemple). Ce phénomène est appelé piégeage ionique. Il explique des concentrations plus importantes dans certains compartiments en fonction du pH.