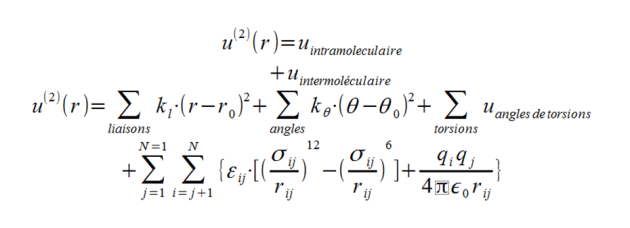Interactions et mouvement des noyaux atomiques
Approximation de Born Oppenheimer :
La mécanique moléculaire s'intéresse aux noyaux atomiques en considérant qu'ils possèdent chacun une distribution fixe d'électrons.
La mécanique moléculaire utilise alors les lois de la mécanique classique rappelées auparavant.
interactions entre particules : les champs de force
Interactions → concepts mécaniques = centres atomiques reliés par des liaisons chimiques explicites.
Etotale = E"liantes" intramoléculaires + E "non liantes" intermoléculaires.
Energie intramoléculaire ou interaction liante :
Degrés de liberté = élongation des liaisons + pliage + torsion
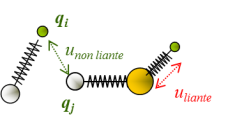
Energie intermoléculaire ou interaction non-liante :
La forme fonctionnelle, souvent en puissance inverse de la distance indique la portée (grande portée pour 1/r, moyenne pour 1/r3, courte pour 1/r6, très faible pour 1/r12).
Eintermoléculaire = somme de potentiels d'interaction de paire.
Les interactions électrostatiques = interaction coulombienne en 1/r entre deux charges ponctuelles + interactions entre dipôle - charge en 1/r2 (dipôle fixe) ou 1/r4 (dipôle mobile) + interactions entre dipôle - dipôle fixes en 1/r3 ou entre quadrupôles (comme dans le CO2).
Les interactions faibles de type van der Waals = interactions répulsives et attractives entre deux atomes.
ex. potentiel de Lennard Jones '12-6'.
ce sont les interactions de type van der Waals qui sont principalement considérées dans ce module par la suite